Titanium
Titanium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Ti dan nomor atom 22.
Bentuk Fisik
Unsur ini merupakan logam transisi yang ringan, kuat, berkilau, tahan korosi (termasuk tahan terhadap air laut, aqua regia HNO3 + 3HCl dan klorin) dengan warna putih-metalik-keperakan.
Kegunaan Titanium
- Perikanan: karena sifat Titanium yang kuat, ringan, dan tahan korosif air laut jadi untuk pembuatan pancingan.
- Industri: beberapa mesin pemindah panas (heat exchanger)dan bejana bertekanan tinggi serta pipa-pipa tahan korosi memakai bahan titanium.
- Militer: oleh karena kekuatannya, unsur ini digunakan untuk membuat peralatan perang (tank) dan untuk membuat pesawat ruang angkasa.
- Kedokteran: bahan implan gigi, penyambung tulang, pengganti tulang tengkorak, struktur penahan katup jantung.
- Mesin: material pengganti untuk batang piston.
Sifat Fisika
Fase: solid
Titik lebur: 1941 K (1668 °C, 3034 °F)
Titik didih: 3560 K (3287 °C, 5949 °F)
Kepadatan mendekati s.k.: 4.506 g/cm3
saat cair, pada t.l. 4.11 g/cm3
Kalor peleburan: 14.15 kJ/mol
Kalor penguapan: 425 kJ/mol
Kapasitas kalor molar: 25.060 J/(mol·K)

Sifat Atom
Bilangan oksidasi: 4, 3, 2, 1 oksida amfoter
Elektronegativitas Skala Pauling: 1.54
Energi ionisasi: (artikel)
Jari-jari atom empiris: 147 pm
Jari-jari kovalen: 160±8 pm
Senyawa Titnium
Bilangan oksidasi +4 mendominasi unsur titanium, tetapi senyawa pada bilangan oksidasi +3 juga banyak ditemukan. Umumnya, titanium mempunyai geometri koordinasi oktahedral pada kompleksnya, tetapi TiCl4 yang tetrahedral adalah pengecualian.
Karena bilangan oksidasinya tinggi, senyawa titanium(IV) memiliki sifat ikatan kovalen tinggi. Tidak seperti logam transisi lain, kompleks aquo Ti(IV) tidak diketahui.
Oksida
Oksida yang paling penting adalah TiO2, yang ada pada 3 polimorf; anatase, brookite dan rutile. Ketiganya adalah padatan diamagnetik warna putih, meski ada beberapa sampelnya berwarna gelap.
Titanat biasanya merujuk ke senyawa titanium(IV), seperti barium titanat (BaTiO3). Dengan struktur perovskite, material ini memiliki sifat piezoelektrik dan digunakan sebagai transduser pada interkonversi suara dan kelistrikan. Banyak mineral merupakan titanat, seperti ilmenit (FeTiO3). Safir bintang dan rubi memiliki sifat asterisme dari adanya titanium dioksida didalamnya.
Beberapa macam oksida tereduksi dari titanium telah diketahui. Ti3O5 adalah semikonduktor warna ungu yang diproduksi dari reduksi TiO2 dengan hidrogen pada suhu tinggi,[12] dan digunakan pada industri ketika ada permukaan yang perlu di-vapour-coated dengan titanium dioksida: akan menguap sebagai TiO murni, sedangkan TiO2 menguap sebagai campuran oksida dan dan pelapisan deposit dengan indeks refraktif bervariasi. Juga senyawa yang dikenal adalah Ti2O3, dengan struktur karborundum dan TiO.
Alkoksida
Alkoksida dari titanium(IV), dibuat dengan mereaksikan TiCl4 dengan alkohol, adalah senyawa tak berwarna yang akan berubah menjadi dioksida ketika direaksikan dengan air. Dalam industri hal ini berguna untuk mendapatkan padatan TiO2 via proses sol-gel. Titanium isopropoksida digunakan dalam sintesis senyawa organik kiral melalui proses sharpless.
Sulfida
Titanium membentuk berbagai macam varietas sulfida, namun hanya TiS2 yang menarik perhatian. Senyawa ini digunakan sebagai katoda dalam pengembangan baterai litium. Karena Ti(IV) adalah “kation berat”, sulfida titanium tidak stabil dan cenderung terhidrolisis dengan pelepasan hidrogen sulfida.
Isotop Titanium
Isotop Titanium terstabil
| Isotop | Kelimpahan | Waktu paruh (t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 44Ti | syn | 63 y | ε | 44Sc | |
| γ | – | ||||
| 46Ti | 8.0% | 46Ti stabil dengan 24 neutron | |||
| 47Ti | 7.3% | 47Ti stabil dengan 25 neutron | |||
| 48Ti | 73.8% | 48Ti stabil dengan 26 neutron | |||
| 49Ti | 5.5% | 49Ti stabil dengan 27 neutron | |||
| 50Ti | 5.4% | 50Ti stabil dengan 28 neutron | |||
Sejarah Titanium
Titanium ditemukan di Cornwall, Kerajaan Britania Raya pada tahun 1791 oleh William Gregor dan dinamai oleh Martin Heinrich Klaproth dari mitologi Yunani Titan. Elemen ini ada di antara deposit-deposit berbagai mineral, diantaranya rutile dan ilmenit, yang banyak terdapat pada kerak bumi dan litosfer, serta pada hampir semua makhluk hidup, batuan, air, dan tanah.
Logam ini diekstrak dari bijih mineralnya melalui proses Kroll[3] atau proses Hunter. Senyawanya yang paling umum, titanium dioksida, adalah fotokatalisator umum dan digunakan dalam pembuatan pigmen putih. Senyawa lainnya adalah titanium tetraklorida (TiCl4), komponen layar asap dan katalis; dan titanium triklorida (TiCl3), digunakan sebagai katalis dalam produksi polipropilena.

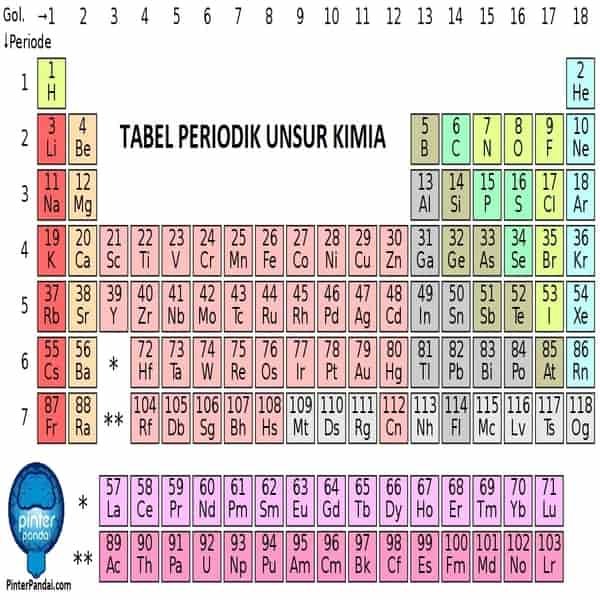
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya