Skandium
Skandium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Sc dan nomor atom 21.
Skandium berupa logam transisi yang lembut dan warnanya putih keperakan, merupakan mineral yang langka dari Skandinavia dan kadang-kadang diklasifikasikan bersama yttrium dan lantanida sebagai elemen mineral langka.
Bentuk Fisik Skandium
Skandium adalah logam yang cukup lembut dan berwarna putih keperakan.
Kegunaan Skandium
Skandium adalah salah satu bahan kimia langka, yang digunakan pada berbagai perkakas seperti televisi warna, lampu neon, lampu hemat energi, dan kacamata.
Penggunaan skandium masih terus berkembang mengingat unsur ini cocok untuk memproduksi catalyser serta untuk memoles kaca.
Aplikasi utama skandium adalah untuk membuat paduan aluminium-skandium yang digunakan oleh industri kedirgantaraan dan peralatan olahraga (sepeda, tongkat bisbol, dll) yang membutuhkan material kinerja tinggi.
Sifat Fisika
Fase: solid
Titik lebur: 1814 K (1541 °C, 2806 °F)
Titik didih: 3109 K (2836 °C, 5136 °F)
Kepadatan mendekati s.k.: 2.985 g/cm3
saat cair, pada t.l.: 2.80 g/cm3
Kalor peleburan: 14.1 kJ/mol
Kalor penguapan: 332.7 kJ/mol
Kapasitas kalor molar: 25.52 J/(mol·K)
Sifat Atom
Bilangan oksidasi 3, 2, 1 oksida amfoter
Elektronegativitas Skala Pauling: 1.36
Energi ionisasi
Jari-jari atom empiris: 162 pm
Jari-jari kovalen: 170±7 pm
Jari-jari van der Waals: 211 pm

Isotop Skandium
Di alam, skandium ada dalam bentuk satu isotop stabil yaitu skandium-45. Di antara 25 (tidak termasuk isomer nuklir) isotop radioaktif dengan massa antara 36 sampai 61, yang paling stabil adalah skandium-46 (paruh 83,79 hari). Yang paling stabil adalah skandium-39 (waktu paruh kurang dari 300 nanodetik).
Isotop Skandium terstabil
| Isotop | Kelimpahan | Waktu paruh(t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 44mSc | syn | 58.61 h | IT | 44Sc | |
| γ | 44Sc | ||||
| ε | 44Ca | ||||
| 45Sc | 100% | 45Sc stabil dengan 24 neutron | |||
| 46Sc | syn | 83.79 d | β− | 46Ti | |
| γ | – | ||||
| 47Sc | syn | 3.3492 d | β− | 47Ti | |
| γ | – | ||||
| 48Sc | syn | 43.67 h | β− | 48Ti | |
| γ | – | ||||
Sejarah Skandium
Setelah ahli kimia Rusia Dmitry Ivanovich Mendeleyev pada tahun 1871 menemukan keberadaan unsur ini dan menyebutnya ekaboron. Kimiawan Swedia Lars Fredrik Nilson pada tahun 1879 menemukan oksidanya yaitu scandia, di tanah yang jarang mineral seperti gadolinit dan euksenit.
Kimiawan Swedia Per Teodor Cleve kemudian pada tahun 1879 mengidentifikasi skandium sebagai ekaboron.
Efek kesehatan
Skandium milik keluarga tanah jarang (lantanida + skandium + Yttrium). Semua tanah jarang memiliki sifat yang sebanding. Tanah jarang pada dasarnya hadir dalam dua jenis bijih: monasit dan bastnaesit. Mereka digunakan dalam katalisis, metalurgi, kaca dan keramik dan juga di lampu tertentu (fluorescent, dll).
Produksi skandium meningkat karena kemungkinan aplikasinya dalam aeronautika.
Skandium kecil ditemukan di alam, karena hadir dalam jumlah kecil.
Skandium terutama berbahaya di tempat kerja, karena Anda dapat menghirup uap dan gasnya dengan udara. Hal ini dapat menyebabkan emboli paru, terutama selama paparan yang lama. Secara umum, skandium dan tanah jarang cenderung menumpuk di hati saat diserap.
Dampak lingkungan
Secara umum, skandium dan tanah jarang dilepaskan ke lingkungan, khususnya oleh industri penghasil bensin (katalis untuk perengkahan, aditif). Tanah jarang juga dilepaskan ke lingkungan ketika peralatan rumah tangga tertentu dibuang (televisi, misalnya).
Skandium secara bertahap terakumulasi di tanah dan perairannya dan, pada akhirnya, konsentrasinya akan meningkat pada manusia, hewan, dan di dalam tanah.
Pada hewan air, skandium menyebabkan kerusakan pada membran sel. Ini memiliki pengaruh negatif pada reproduksi dan fungsi sistem saraf.
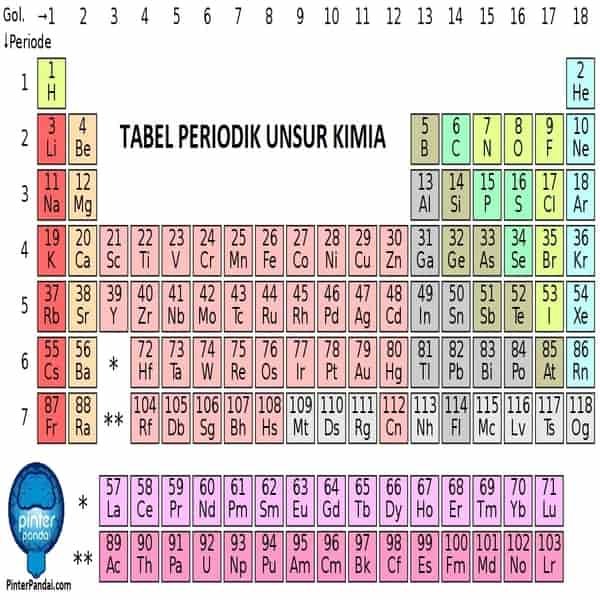
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing