Silikon (Silicon)
Silikon adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Si dan nomor atom 14.
Silikon adalah polimer nonorganik yang bervariasi, dari cairan, gel, karet, hingga sejenis plastik keras. Beberapa karakteristik khusus silikon: tak berbau, tak berwarna, kedap air, serta tak rusakakibat bahan kimia dan proses oksidasi, tahan dalam suhu tinggi, serta tidak dapat menghantarkan listrik.
Fisik Silikon
Silikon berbentuk padat pada suhu ruangan, dengan titik lebur dan titik didih masing-masing 1.400 dan 2.800 derajat celsius. Yang menarik, silikon mempunyai massa jenis yang lebih besar ketika dalam bentuk cair dibanding dalam bentuk padatannya. Tapi seperti kebanyakan substansi lainnya, silikon tidak akan bercampur ketika dalam fase padatnya, tetapi hanya meluas, sama seperti es yang memiliki massa jenis lebih kecil daripada air.
Karena mempunyai konduktivitas thermal yang tinggi (149 W·m−1·K−1), silikon bersifat mengalirkan panas sehingga tidak pernah dipakai untuk menginsulasi benda panas.
Dalam bentuk kristalnya, silikon murni berwarna abu-abu metalik. Seperti germanium, silikon agak kuat tetapi sangat rapuh dan mudah mengelupas. Seperti karbon dan germanium, silikon mengkristal dalam struktur kristal kubus berlian, dengan jarak kisi 0,5430710 nm (5.430710 Å).
Orbital elektron terluar dari silikon mempunyai 4 elektron valensi. Kulit atom 1s,2s,2p, dan 3s terisi penuh, sedangkan kulit atom 3p hanya terisi 2 dari jumlah maksimumnya 6. Dan Silikon bersifat semikonduktor.
Kegunaan Silikon Dalam Kehidupan Sehari-Hari
Silikon sering digunakan untuk membuat serat optik. Untuk tujuan itu diperlukan silikon ultra murni. Silikon juga digunakan dalam berbagai jenis alise dengan besi (baja). Sedangkan senyawa silikon digunakan dalam industri. Silica dan silikat digunakan untuk membuat gelas, keramik, porselin dan semen.
Silikon dapat juga digunakan dalam operasi plastik digunakan untuk mengisi bagian tubuh pasien dalam bentuk silikone.
Isotop Silicon
Silicon merupakan metaloid, siap untuk memberikan atau berbagi 4 atom terluarnya, sehingga memungkinkan banyak ikatan kimia. Meski silikon bersifat relatif inert seperti karbon, silikon masih dapat bereaksi dengan halogen dan alkali encer. Kebanyakan asam (kecuali asam nitrat dan asam hidrofluorat) tidak bereaksi dengan silikon.
Silicon dengan 4 elektron valensinya mempunyai kemungkinan untuk bergabung dengan elemen atau senyawa kimia lainnya pada kondisi yang sesuai.
Silicon yang eksis di alam terdiri dari 3 isotop yang stabil, yaitu silikon-28, silikon-29, dan silikon-30, dengan silikon-28 yang paling melimpah (92% kelimpahan alami). Dari jumlah tersebut, hanya silikon-29 yang hanya digunakan di dalam spektroskopi NMR dan EPR.
Dua puluh radioisotop telah diketahui, dengan silikon-32 sebagai yang paling stabil dengan paruh waktu 170 tahun dan silikon-31 dengan waktu paruh 157,3 menit. Sisa isotop radioaktif lainnya mempunyai paruh waktu kurang dari 7 detik dan kebanyakan malah kurang dari 0,1 detik. Silikon tidak mempunyai isomer nuklir.
Isotop dari Silicon mempunyai nomor massa berkisar antara 22 sampai 44. Bentuk peluruhan paling umum dari 6 isotop yang nomor massanya dibawah isotop paling stabil (silikon-28) adalah β+, utamanya membentuk isotop aluminium (13 proton) sebagai produk peluruhannya.Untuk 16 isotop yang nomor massanya diatas 28, bentuk peluruhan paling umumnya adalah β−, utamanya membentuk isotop fosfor (15 proton) sebagai produk peluruhan.
Isotop Silicon terstabil
| Isotop | Kelimpahan | Waktu paruh (t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 28Si | 92.23% | 28Si stabil dengan 14 neutron | |||
| 29Si | 4.67% | 29Si stabil dengan 15 neutron | |||
| 30Si | 3.1% | 30Si stabil dengan 16 neutron | |||
| 32Si | sisa | 170 y | β− | 32P | |

Senyawa Silikon
Sebagian besar senyawa silikon digunakan di industri tanpa dipisahkan menjadi elemennya. Lebih dari 90% kerak bumi terdiri dari mineral silikat yang merupakan senyawa silikon dan oksigen. Banyak dari mineral ini digunakan langsung, seperti tanah liat, pasir silika, dan berbagai jenis batuan untuk bangunan. Silika juga menjadi bahan utama batu keramik.
Silikat digunakan dalam pembuatan semen Portland yang digabung dengan pasir silika dan gravel untuk membentuk beton, basis hampir semua bangunan industri modern saat ini.
- Silicon membentuk senyawa biner yang disebut dengan silisida dengan banyak elemen logam yang nantinya menghasilkan senyawa dengan sifat yang beragam, misalnya magnesium silisida, Mg2Si yang sangat reaktif sampai senyawa tahan panas seperti molibdenum disilisida, MoSi2.[27]
- Silicon karbida, SiC (karborundum) adalah padatan keras, tahan panas.
- Silicon SiH4, adalah gas firoforik dengan struktur tetrahedral mirip dengan metana, CH4. Senyawa murninya sendiri tidak bereaksi dengan air ataupun asam lemah, tetapi jika bereaksi dengan alkali maka langsung akan terjadi hidrolisis. Ada kelompok silikon hidrida terkatenasi yang membentuk senyawa yang homolog, SinH2n+2 dengan n berkisar 2–8. Semua senyawa ini mudah terhidrolisis dan tidak stabil, terutama pada senyawa suku tinggi.[29][30]
- Disilena, senyawa yang berisi ikatan rangkap dua silikon-silikon (mirip alkena) dan secara umum sangat reaktif, memerlukan gugus subtituen yang besar untuk menstabilkannya.
- Disiluna, senyawa dengan silikon-silikon rangkap tiga pertama kali didapatkan tahun 2004, meski senyawanya berbentuk non-linear, ikatannya tidak sama dengan alkuna.
- Tetrahalida, SiX4, adalah senyawa yang dapat dibentuk dengan semua halogen. Silicon tetraklorida, misalnya, dapat bereaksi dengan air, tak sama dengan homolognya, karbon tetraklorida. Silicon dihalida dapat dibentuk dengan reaksi dengan suhu tinggi antara silikon dan tetrahalida; dengan struktur yang serupa dengan karbena sehingga senyawa ini adalah senyawa reaktif. Silikon difluorida terkondensasi untuk membentuk senyawa polimer(SiF2)n.[30]
- Silicon dioksida adalah padatan tahan panas berbentuk kristal; mineral yang paling umum adalah quartz. Pada mineral quartz, setiap atom silikon dikelilingi oleh empat atom oksigen yang menjembatani atom silikon lainnya untuk membentuk kisi tiga dimensi.[34] Silika dapat larut dalam air pada suhu tinggi untuk membentuk senyawa asam monosilikat, Si(OH)4.
- Dengan kondisi yang sesuai, asam monosilikat dapat terpolimer untuk membentuk asam silikat yang lebih kompleks, muali dari senyawa kondensasi paling sederhana, asam disilikat (H6Si2O7) sampai struktur kompleks yang menjadi basis banyak mineral silikat yang disebut asam polisilikat {Six(OH)4–2x}n.
SilikSilikon murni berwujud padat seperti logam dengan titik lebur 14100C. silikon dikulit bumi terdapat dalam berbagai bentuk silikat, yaitu senyawa silikon dengan oksigen. Unsur ini dapat dibuat dari silikon dioksida (SiO2) yang terdapat dalam pasir, melalui reaksi:
SiO2(s)+ 2C(s)→ Si(s) + 2CO(g)
Silikon murni berstruktur seperti Intan ( tetrahedral) sehingga sangat keras dan tidak menghantarkan listrik, jika dicampur dengan sedikit unsur lain, seperti alumunium (Al) atau boron (B). Silicon bersifat semikonduktor (sedikit menghantarkan listrik), yang diperlukan dalam berbagai peralatan, elektronik, seperti kalkulator dan Komputer. Itulah sebabnya silikon merupakan zat yang sangat penting dalam dunia modern. Untuk itu dibutuhkan silikon yang kemurniannya sangat tinggi dan dapat dihasilkan dengan reaksi:
SiCl4(g) + 2H2(g) → Si(s) + 4HCl(g)
Jari-jari silikon lebih besar dari karbon, sehingga tidak dapat membentuk ikatan π (rangkap dua atau tiga) sesamanya, hanya ikatan tunggal (σ). Karena itu silikon tidak reaktif pada suhu kamar dan tidak bereaksi dengan asam, tetapi dapat bereaksi dengan basa kuat seperti NaOH.
Si(s) + 4OH–(aq) → SiO4(aq) + 2H2(g)
Pada suhu tinggi, silikon dapat bereaksi dengan hidrogen membentuk hidrida, dan dengan halogen membentuk halide, seperti:
Si(s) + 2H2 → SiH4
Si(s) + 2Cl2 → SiCl4

Sejarah Silikon
Silika adalah salah satu benda berstruktur tajam pertama yang dibuat oleh manusia. Pada peradaban kuno orang-orang sebenarnya telah menggunakan silika yang didapat dari batu kristal.
Unsur kimia ini ditemukan oleh Jons Jakob Berzelius tahun 1824. Terdapat dialam dalam bentuk tanah liat, granit, kuartza dan pasir, kebanyakan dalam bentuk silikon dioksida (dikenal sebagai silika) dan dalam bentuk silikat.
Efek Kesehatan
Unsurnya adalah bahan inert, yang tidak memiliki sifat menyebabkan fibrosis paru-paru. Namun, kerusakan paru-paru ringan telah dilaporkan pada hewan laboratorium dengan injeksi debu silikon intratrakeal. Debu silikon memiliki sedikit efek pada paru-paru dan tampaknya tidak menimbulkan penyakit atau efek toksik yang signifikan jika paparan tetap minimal.
Silikon dapat menyebabkan efek pernapasan kronis. Silika kristal (silikon dioksida) dapat menyebabkan bahaya pernapasan yang signifikan. Namun, kemungkinan pembentukan silika kristalin selama proses normal sangat rendah. LD 50 (oral) – 3160 mg/kg. (LD50: Dosis Mematikan 50: Dosis suatu zat yang menyebabkan kematian 50% populasi hewan yang terpapar zat tersebut melalui rute apa pun selain penghirupan. Biasanya dinyatakan sebagai miligram atau gram bahan per kilogram berat hewan).
Silika kristal mengiritasi kulit dan mata saat kontak. Inhalasi menyebabkan iritasi paru-paru dan pembentukan lendir pada selaput. Kontak dengan mata dapat menyebabkan kemerahan. Kemerahan, pengelupasan dan gatal-gatal adalah ciri-ciri peradangan kulit.
Kanker paru-paru dikaitkan dengan paparan silika kristal dan lebih khusus lagi kuarsa dan kristobalit. Hubungan paparan-respons telah dilaporkan dalam studi penambang, pekerja granit, pekerja tembikar, pekerja bata api, dll.
Beberapa studi epidemiologi telah menunjukkan statistik yang signifikan dari kematian atau kasus gangguan imunologi dan penyakit autoimun pada pekerja yang terpapar silika. Penyakit dan gangguan ini termasuk skleroderma, rheumatoid arthritis, lupus, dan sarkoidosis.
Studi epidemiologi baru-baru ini telah menunjukkan hubungan yang signifikan secara statistik dari paparan kerja terhadap silika kristalin dengan penyakit ginjal dan perubahan ginjal subklinis.
Silika kristal dapat mempengaruhi sistem kekebalan tubuh, menyebabkan infeksi mikobakteri (TB dan non-TB) atau jamur, terutama pada pekerja dengan silikosis.
Paparan silika kristal di tempat kerja dikaitkan dengan bronkitis, penyakit paru obstruktif kronik (PPOK) dan emfisema. Beberapa studi epidemiologi menunjukkan bahwa efek kesehatan ini mungkin kurang sering atau tidak ada pada non-perokok.
Efek pada lingkungan
Tidak ada efek negatif pada lingkungan yang dilaporkan.
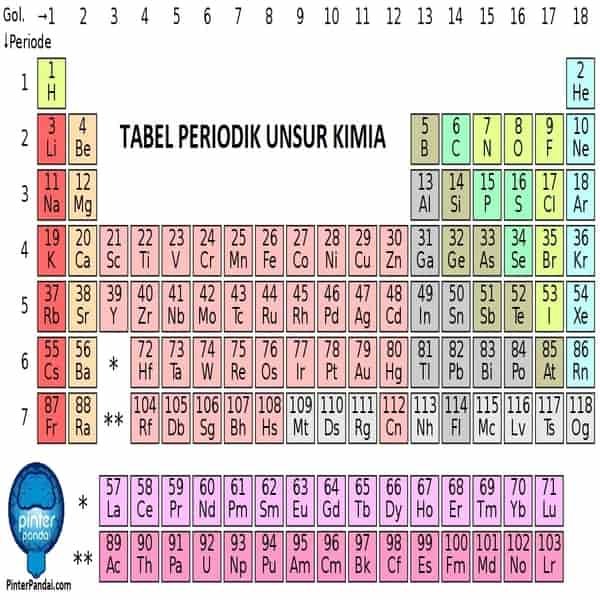
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Manfaat Emas Dalam Pengobatan Kesehatan Medis
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing