Senyawa Biner
Sebuah senyawa biner adalah senyawa kimia yang mengandung 2 unsur yang berbeda.
Contohnya: air (H2O), amonia (NH3) dan metana (CH4). Ketiga senyawa tersebut hanya tersusun atas dua jenis unsur yaitu hidrogen dan oksigen pada senyawa air, nitrogen dan hidrogen pada amonia serta karbon dan hidrogen pada metana. Berdasarkan jenis ikatannya, senyawa biner dibedakan menjadi dua jenis yaitu senyawa biner ionik dan senyawa biner kovalen.
Asam biner
Dalam kelompok senyawa biner hidrogen, sebuah asam biner meliputi sebuah atom hidrogen yang terikat pada atom lain yang biasanya berada pada golongan 7 tabel periodik. Termasuk di dalamnya adalah klorin, fluorin, bromin, iodin, dan astatin. Termasuk pula unsur lain seperti belerang, telurium, polonium, selenium, dan arsenik.
Konvensi penamaannya (dalam Bahasa Inggris) adalah:
“Hydro-” + Nonlogam + “-ic” + “acid”
Contohnya adalah HCl: hydrochloric acid atau yang dalam Bahasa Indonesia dikenal dengan asam klorida.
Jika asamnya berada dalam bentuk gas atau anhidrat, akhiran “-ic” diganti dengan “-ide” dan kata-kata “acid” dihilangkan.

Senyawa kovalen biner
Bahasa Inggris: Nonmetal X + Nonmetal Y + “-ide.” Bahasa Indonesia: Nonlogam X + Nonlogam Y + “-ida.”
Tambahkan awalan Latin yang sesuai pada masing-masing nama unsur untuk menyatakan jumlah atom masing-masing unsur yang terdapat dalam molekul senyawa tersebut.
Metode ini umumnya tidak digunakan untuk senyawa ionik (lihat di bawah). Misalnya, K2O biasanya tidak disebut sebagai dikalium monoksida (dipotassium monoxide); tetapi cukup disebut kalium oksida (potassium oxide). Alasan disebut kalium oksida adalah bahwa kalium oksida merupakan senyawa ionik biner, sehingga mengikuti aturan untuk senyawa ionik biner. Namun, P4O6 disebut tetrafosfor heksosida (tetraphosphorus hexoxide). Beberapa unsur yang dimulai dengan vokal (Oksigen, misalnya) menggantikan vokal di akhir awalannya; mono- + oksida = monoksida, O4 = tetroksida, O5 = pentoksida, dan seterusnya.
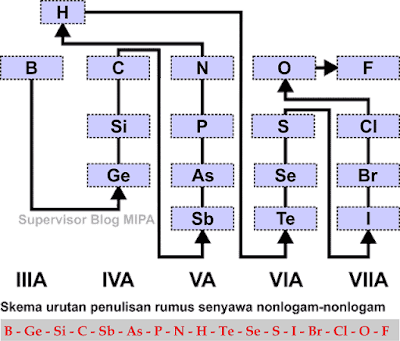
1. Penulisan Rumus Senyawa Nonlogam-Nonlogam
2. Nama Senyawa Nonlogam-Nonlogam
1 | = | Mono | 6 | = | Heksa |
2 | = | Di | 7 | = | Hepta |
3 | = | Tri | 8 | = | Okta |
4 | = | Tetra | 9 | = | Nona |
5 | = | Penta | 10 | = | Deka |
N2O | : | Dinitrogen monoksida |
NO | : | Nitrogen monoksida (bukan mononitrogen monoksida) |
NO2 | : | Nitrogen dioksida (bukan mononitrogen dioksida) |
N2O5 | : | Dinitrogen pentaoksida |
HCl | : | Hidrogen klorida atau asam klorida (bukan hidrogen monoklorida) |
HF | : | Hidrogen fluorida atau asam fluorida (bukan hidrogen monofluorida) |
HBr | : | Hidrogen bromida atau asam bromida (bukan hiroden monobromida) |
H2S | : | Hidrogen sulfida atau asam sulfida (bukan dihidrogen monosulfida) |
3. Senyawa Umum
H2O | : | Air (bukan hidrogen oksida) |
NH3 | : | Amonia (bukan nitrogen trihidrida) |
CH4 | : | Metana (bukan karbon tetrahidrida) |
Senyawa ionik biner
Sebuah senyawa ionik biner adalah garam yang mengandung hanya dua unsur yang keduanya berupa ion, sebuah kation (yang memiliki muatan positif) dan sebuah anion (yang mempunyai muatan negatif). Ketika memberi nama senyawa-senyawa ini, komposisinya harus diperhatikan. Senyawa ionik biner tipe 1 adalah senyawa-senyawa yang kationnya hanya memiliki satu bentuk, atau muatan.
Senyawa ionik biner tipe 2 adalah senyawa-senyawa yang kationnya dapat memiliki beberapa bentuk:
- Kation (dalam banyak kasus adalah logam) didaftarkan pertama dan anion (yang umumnya nonlogam) didaftarkan kedua.
- Kation mengambil nama bentuk unsurnya. Misalnya, Li+ disebut sebagai “Litium”.
- Nama anion menggunakan bagian awal nama unsurnya, dan dilanjutkan dengan penambahan akhiran “-ida”. Misalnya, Br− akan disebut sebagai “Bromida”. Contoh: LiF (yang tersusun dari kation Li+ dan anion F−) = litium fluorida; BaO (yang tersusun dari kation Ba2+ dan anion O2−) = barium oksida.
Jika logam yang digunakan adalah logam transisi kecuali Al3+, Zn2+, Ag+, tahapannya mengikuti pola seperti senyawa ionik biner tipe 1, tetapi, karena kationnya dapat mengalami berbagai tingkat muatan, muatannya harus ditulis di dalam kurung dalam huruf Romawi di belakang nama kationnya. Contohnya: CoO (yang tersusun atas kation Co2+ dan anion O2−) = kobalt(II) oksida; FeN (yang tersusun dari kation Fe3+ dan anion N3−) = besi(III) nitrida.
Perlu dicatat bahwa ada cara lain dalam memberi nama senyawa ionik biner tipe 2 yang tidak umum. Ini melibatkan penggunaan nama Latin untuk kationnya. Kation tipe 2 yang umum meliputi besi, tembaga, kobalt, timah, timbal, dan raksa.
Kation + Anion + “-ida” (untuk anion yang mengandung unsur tunggal, misalnya nitrida).
Jika dimungkinkan terdapat banyak senyawa, tingkat oksidasi kation ditambahkan di belakangnya dalam angka Romawi (tembaga(II) sulfat), atau nama kation (dalam bahasa Latin) diberi akhiran “-o” (untuk tingkat oksidasi yang lebih rendah) atau “-i” (untuk tingkat oksidasi yang lebih tinggi). Sebagai contoh: tembaga(I) sulfida = kupro sulfida, tembaga(II) sulfida = kupri sulfida.
1. Penulisan Rumus Senyawa Logam-Nonlogam
2. Nama Senyawa Logam-Nonlogam
KBr | : | Kalium bromida (bukan kalium monobromida) |
MgBr2 | : | Magnesium bromida (bukan magnesium dibromida |
Cu2O | : | Tembaga (I) oksida |
CuO | : | Tembaga (II) oksida |
FeCl2 | : | Besi (II) klorida |
FeCl3 | : | Besi (III) klorida |
4. Tabel Penamaan Kation dan Anion Beberapa Unsur
Kation | Nama | Anion | Nama |
Na+ | Natrium | H– | Hidrida |
K+ | Kalium | N3- | Nitrida |
Rb+ | Litium | O2- | Oksida |
Cs+ | Sesium | S2- | Sulfida |
Mg2+ | Magnesium | F– | Fluorida |
Ca2+ | Kalsium | Cl– | Klorida |
Sr2+ | Stronsium | Br– | Bromida |
Ba2+ | Barium | I– | Iodida |
Al3+ | Aluminium | Se2- | Selenida |
Zn2+ | Seng | P3- | Fosfida |
Ag+ | perak | As3- | Arsenida |
Contoh Soal dan Jawaban Senyawa Biner – Asam, Kovalen dan Ionik
1. Berilah nama pada senyawa berikut ini
a)NaBr
2. Tuliskan rumus senyawa dari nama-nama senyawa berikut:
Jenis Senyawa : Asam, Basa, Ionik, Garam, Oksida dan Organik

Klik disini untuk mengetahui jenis-jenis senyawa lainnya.
- Jenis Senyawa : Asam, Basa, Ionik, Garam, Oksida dan Organik
- Asam Basa pH – Rumus Kimia, Penjelasan, Contoh Soal dan Jawaban
- Asam Basa Konjugat – Konjugasi Asam Basa & Rumus, Konjugat, Contoh Soal dan Jawaban
- pH Derajat Keasaman, p[H], pOH – Rumus, Soal dan Jawaban
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Surfaktan Senyawa Organik – Penjelasan, Contoh Soal dan Jawaban
- Nama Obat dan Untuk Penyakit Apa ? – Daftar Nama Obat Esensial diterbitkan oleh Organisasi Kesehatan Dunia (WHO)
- Fraksi Mol Kimia”Xi” – Rumus, Penjelasan, Contoh Soal dan Jawaban
- 10 Kegiatan Yang Akan Membantu Otak Anda Menjadi Tetap Muda Dan Tajam
- Apa Yang Terjadi Pada Saat Otak Kita Membeku?
- Sifat (perilaku) dapat dirubah. Tetapi watak (karakter) tidak dapat. Setuju ???
- Ternyata, jatuh cinta sebabkan perubahan kimiawi pada otak – hormon serotonin
- Cara Berciuman – Tips, Nasihat Dan Langkah Untuk Ciuman Pertama Yang Sempurna
- 7 Cara Untuk Menguji Apakah Dia, Adalah Teman Sejati Anda Atau Bukan BFF (Best Friend Forever)
- Kepalan Tangan Menandakan Karakter Anda – Kepalan nomer berapa yang Anda miliki?
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan sering terdengar jika Anda memasang applikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Britannica, Science Direct, LibreTexts, Elementalmatter
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya | Business & Marketing