Raksa
Raksa adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Hg dan nomor atom 80.
Raksa / merkuri adalah cairan logam perak atau disebut air raksa (Hydrargyrum ). Merkuri merupakan unsur transisi dalam susunan tabel periodik unsur, di mana merkuri ada pada golongan II B dan periode 6.
Bentuk Fisik
Logam murninya keperakan, cairan, tak berbau, dan mengkilap. Bila dipanaskan pada suhu 3570C akan menguap. Merkuri banyak ditemukan di alam dan tersebar dalam batu-batuan, biji tambang, tanah, air dan udara sebagai senyawa anorganik dan organik.
Kegunaan Raksa
Digunakan dalam termometer, barometer dan beberapa jenis baterai. Juga digunakan dalam listrik switch dan produk lampu uap raksa.
Dalam dunia keindustrian, air raksa digunakan sebagai elektroda cair dalamm pembuatan kalium dan natrium hidroksida melalui proses elektrolisis garam. Unsur berlambang Hg ini juga digunakan dalam beberapa peralatan listrik seperti saklar, rectifier, dan sebagai katalis reaksi.
Beberapa senyawa yang mengandung air raksa mempunyai manfaat. Kalomel (Hg2Cl2) digunakan sebagai standar dalam pengukuran elektrokimia dan obat pencahar. Merkuri Klorida digunakan sebagai racun pembunuh serangga, tikus, dan diinfektan. Senyawa oksida dari air raksa juga digunakan dalam salep kulit. Merkuri sulfat digunakan sebagai katalis dalam reaksi kimia organik.
Senyawa Raksa / Merkuri
Senyawa air raksa di alam jumlahnya terbatas. Senyawa ini ditemukan secara alami dalam bentuk senyawa loga, senyawa garam merkuri, dan senyawa raksa organik. Sumber utama air raksa adalah senyawa HgS. Produksi air raksa di dunia mencapai 8000 ton pertahun.
Unsur air raksa bisa dihasilkan secara alami melalui proses alam dan juga hasil dari aktivitas manusia. Secara alami, raksa dihasilkan dari perusakan mineral di bebatuan dan tanah akibat terpaan angin dan air. Jumlahnya cenderung tetap setiap tahunnya. Sebagian besar air raksa dilepaskan ke alam akibat aktivitas manusia seperti pembakaran bahan bakar fosil, hasil tambang dan pembakaran sampah.
Merkuri / raksa ada pada berbagai tingkat oksidasi:
- 0 (metalik raksa)
- I (ion beraksa Hg22+, Hg2SO4)
- II (ion beraksa Hg2+, HgO, HgSO3, HgI+, HgI2, HgI3–, HgI42-)

Cinnabar kadang-kadang berubah menjadi merkuri asli di zona teroksidasi endapan merkuri.
Isotop Raksa
Isotop Raksa terstabil
| Isotop | Kelimpahan | Waktu paruh(t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 194Hg | syn | 444 y | ε | 194Au | |
| 195Hg | syn | 9.9 h | ε | 195Au | |
| 196Hg | 0.15% | 196Hg stabil dengan 116 neutron | |||
| 197Hg | syn | 64.14 h | ε | 197Au | |
| 198Hg | 9.97% | 198Hg stabil dengan 118 neutron | |||
| 199Hg | 16.87% | 199Hg stabil dengan 119 neutron | |||
| 200Hg | 23.1% | 200Hg stabil dengan 120 neutron | |||
| 201Hg | 13.18% | 201Hg stabil dengan 121 neutron | |||
| 202Hg | 29.86% | 202Hg stabil dengan 122 neutron | |||
| 203Hg | syn | 46.612 d | β− | 203Tl | |
| 204Hg | 6.87% | 204Hg stabil dengan 124 neutron | |||
Sejarah Raksa / Merkuri
Mercury telah di temukan di Mesir pada makam kuno peniggalan abad ke 1500 SM, dan mungkin digunakan untukkeperluan kosmetik dan obat. Sekitar 350 SM, filsuf dan ilmuwan Yunani Aristotel menjelaskan bagaimana caramengambil air raksa dengan memanaskan batuan cinnabar untuk upacara keagamaan. Di Roma, air raksa digunakanuntuk berbagai keperluan dan memberikannya nama hydrargyrum, yang berarti perak cair menjadi asal simbolkimia Hg untuk air raksa.
Tindakan percampuran Mercury pertama kali untuk mengolah ores perak dengan proses patio 1557 di Meksiko membuat permintaan air raksa sangat meningkat. Barometer raksa ditemukan oleh Torricellidi 1643, diikuti oleh penemuan yang raksa termometer oleh Fahrenheit di 1714. Namun kini, dengan alasankesehatan dan keamanan karena sifat toksik yang dimilikinya. penggunaannya untuk bahan pengisi termometer telahdigantikan (oleh termometer alkohol, digital atau termistor).
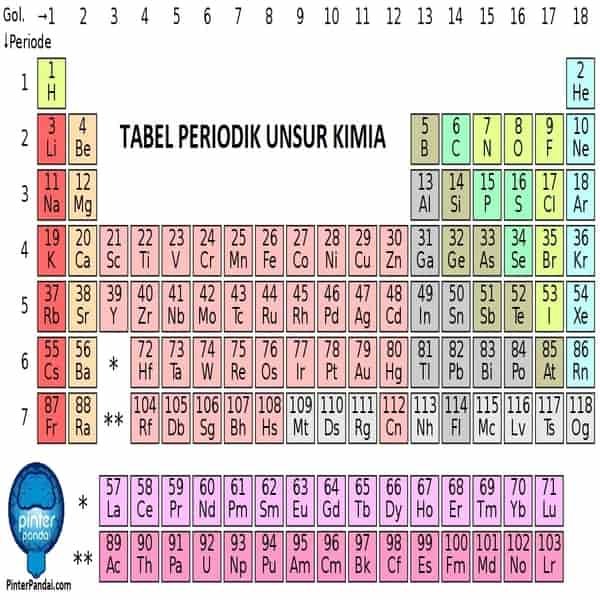
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Libretexts, Royal Society of Chemistry
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya