Kalsium
Kalsium adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Ca dan nomor atom 20.
Mempunyai massa atom 40.078 amu. Kalsium merupakan salah satu logam alkali tanah dan merupakan elemen terabaikan kelima terbanyak di bumi. Kalsium juga merupakan ion terabaikan kelima terbanyak di air laut dilihat dari segi molaritas dan massanya, setelah natrium, klorida, magnesium dan sulfat.
Fisik Kalsium
Kalsium reaktif dan untuk ukuran logam termasuk lembut. Dengan sedikit usaha, bisa dipotong dengan pisau tajam.Dalam kontak dengan udara, kalsium mengembangkan campuran oksida dan pelapisan nitrida, yang melindunginya dari korosi lebih lanjut.Kalsium bereaksi mudah dengan air dan asam dan logam terbakar terang di udara, terutama membentuk nitrida.

Kegunaan Kalsium Dalam Kehidupan Sehari-Hari
Penggunaan kalsium terbesar adalah pembuatan baja, karena afinitas kimiawi yang kuat untuk oksigen dan belerang. Oksida dan sulfidanya, sekali terbentuk, memberi alumina kapur cair dan inklusi sulfida pada baja yang mengapung; Pada perawatan, inklusi ini menyebar ke seluruh baja dan menjadi kecil dan bulat, meningkatkan castability, kebersihan dan sifat mekanik umum.
Kalsium juga digunakan dalam baterai otomotif bebas perawatan, di mana penggunaan paduan kalsium-timah 0,1% dan bukan paduan antimoni-timbal yang biasa menyebabkan hilangnya air yang lebih rendah dan pemakaian self-discharge yang rendah.
Banyak senyawa kalsium yang digunakan dalam makanan, obat-obatan. Sebagai contoh, kalsium dan fosfor ditambahkan dalam makanan melalui penambahan kalsium laktat, kalsium difosfat dan fosfat trikalsium. Yang terakhir juga digunakan sebagai agen poles dalam pasta gigi dan antasida (zat yang berfungsi untuk menetralisir asam lambung).
Calcium lactobionate adalah bubuk putih yang digunakan sebagai agen suspending untuk obat-obatan. Dalam memanggang, kalsium monofosfat digunakan sebagai zat ragi. Kalsium sulfit digunakan sebagai pemutih dalam pembuatan kertas dan sebagai desinfektan, kalsium silikat digunakan sebagai bahan penguat pada karet dan kalsium asetat adalah komponen damar pengikat dan digunakan untuk membuat sabun metalik dan resin sintetis.
Isotop Kalsium
Kalsium alami adalah campuran dari lima isotop stabil (40Ca, 42Ca, 43Ca, 44Ca, and 46Ca) dan satu isotop dengan waktu paruh begitu lama sehingga dapat dianggap stabil untuk semua keperluan praktis (48Ca, dengan waktu paruh sekitar 4.3 × 1019 tahun). Kalsium adalah unsur pertama (paling ringan) yang memiliki enam isotop alami.
Isotop utama kalsium
| Isotope | Abundance | Waktu paruh (t1/2) | Decay mode | Product |
|---|---|---|---|---|
| 40Ca | 96.941% | stable | ||
| 41Ca | trace | 1.03×105 y | ε | 41K |
| 42Ca | 0.647% | stable | ||
| 43Ca | 0.135% | stable | ||
| 44Ca | 2.086% | stable | ||
| 45Ca | syn | 162.7 d | β− | 45Sc |
| 46Ca | 0.004% | stable | ||
| 47Ca | syn | 4.5 d | β− | 47Sc |
| γ | – | |||
| 48Ca | 0.187% | 6.4×1019 y | β−β− | 48Ti |
Sejarah Kalsium
Senyawa kalsium dikenal selama ribuan tahun, meski susunan kimiawi mereka tidak dipahami sampai abad ke-17. Kapur sebagai bahan bangunan dan sebagai plester untuk patung digunakan sejauh sekitar 7000 SM. Tanggal kiln kapur pertama tanggal kembali ke 2500 SM dan ditemukan di Khafajah, Mesopotamia.
Pada waktu yang hampir bersamaan, gypsum dehidrasi (CaSO4·2H2O) sedang digunakan di Piramid Agung Giza; Bahan ini nantinya akan digunakan untuk plester di makam Tutankhamun. Iklim Italia sekarang lebih hangat daripada di Mesir, orang Romawi kuno malah menggunakan mortir kapur yang dibuat dengan memanaskan batu kapur (CaCO3); Nama “kalsium” itu sendiri berasal dari kata Latin calx “kapur”.
Vitruvius mencatat bahwa kapur yang dihasilkan lebih ringan dari pada batu kapur asli, yang menghubungkannya dengan air mendidih. Pada tahun 1755, Joseph Black membuktikan bahwa ini disebabkan oleh hilangnya karbon dioksida, yang sebagai gas tidak dikenali oleh orang Romawi kuno.
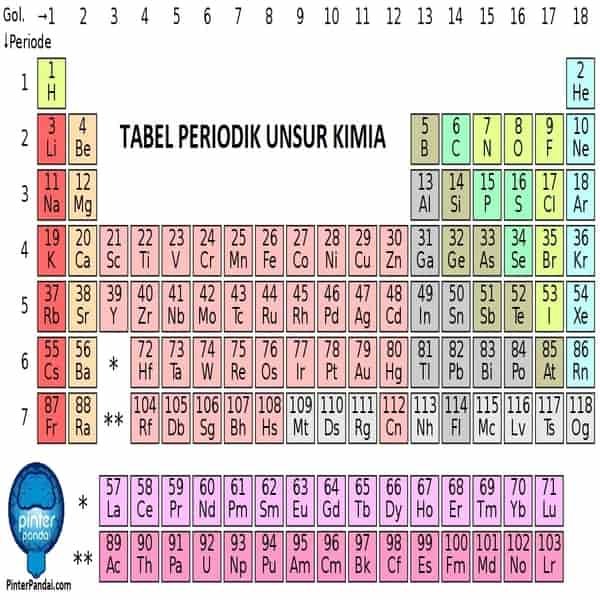
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Wikipedia, Chemistry Explained
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya