Mangan
Mangan adalah suatu unsur kimia dalam tabel periodik yang memiliki lambang Mn dan nomor atom 25.
Mangan relatif melimpah di alam (0,1% kulit bumi). Salah satu sumber manganadalah batuan yang terdapat di dasar lautan dinamakan pirolusit. Suatu batuan yang mengandung campuran mangan dan oksida besi. Kegunaan umum mangan adalah untukmembuat baja yang digunakan untuk mata bor (pemboran batuan).
Kegunaan Mangan
- Saat ini 85-90% produksi mangan masih dikonsumsi industri baja dan untuk keperluan ini biasanya digunakan campuran besi mangan, yaitu feromangan. Feromangan diproduksi dengan mereduksi campuran besi dan oksida mangan dengan karbon. Bijih mangan yang paling utama adalah pirolisit, MnO2.
- Mangan merupakan salah satu produk pertambangan dengan kegunaan luar biasa. Komoditi yang termasuk dalam kelompok dua belas mineral di kulit bumi menjadi bahan baku yang tidak tergantikan di industri baja dunia. Ferro Mangan dan Silico Mangan merupakan dua bentuk mangan yang banyak digunakan industri baja.
- Mangan merupakan salah satu mineral yang digunakan oleh beberapa orang untuk membantu mencegah keropos tulang dan mengurangi gejala yang mengganggu terkait dengan sindrom pramenstruasi (PMS).
- Methylcyclopentadienyl mangan tricarbonyl digunakan sebagai aditif dalam bensin bebas timbel bensin untuk meningkatkan oktan dan mengurangi ketukan mesin. Mangan dalam senyawa organologam yang tidak biasa ini adalah dalam bilangan oksidasi 1.
- Mangan dioksida juga digunakan sebagai katalis.
- Mangan digunakan pula sebagaidekolorisasi kaca dan membuat kaca berwarna ungu.
- Kalium permanganat merupakan oksidator kuat dan digunakan sebagai desinfektan.Senyawa lain yang banyak dimanfaatkan adalah mangan dioksida (MnO) yang digunakanuntuk pupuk dan keramik, serta mangan karbonat (MnCO3) yang dimanfaatkan sebagaimaterial awal untuk membuat senyawa mangan lainnya.
Bentuk Fisik Mangan
Berwarna keperakan dan ini adalah logam keras dan sangat rapuh. Sulit untuk mencair, tapi mudah teroksidasi. Mangan adalah reaktif ketika murni, dan sebagai bedak akan membakar oksigen, bereaksi dengan air (itu berkarat seperti besi) dan larut dalam asam encer.
Sifat Fisika Mangan
Fase: solid
Titik lebur: 1519 K (1246 °C, 2275 °F)
Titik didih: 2334 K (2061 °C, 3742 °F)
Kepadatan mendekati s.k.: 7.21 g/cm3
saat cair, pada t.l.: 5.95 g/cm3
Kalor peleburan: 12.91 kJ/mol
Kalor penguapan: 221 kJ/mol
Kapasitas kalor molar: 26.32 J/(mol·K)
Sifat Atom Mangan
Bilangan oksidasi: 7, 6, 5, 4, 3, 2, 1, -1, -2, -3 oksida amfoter
Elektronegativitas Skala Pauling: 1.55
Energi ionisasi: (artikel)
Jari-jari atom empiris: 127 pm
Jari-jari kovalen: 139±5 (low spin), 161±8 (high spin) pm

Senyawa Mangan
1. Reaksi dengan air
2. Reaksi dengan udara
3. Reaksi dengan halogen
4. Reaksi dengan asam
5. Logam mangan diperoleh dengan
Isotop Mangan
Isotop Mangan terstabil
| Isotop | Kelimpahan | Waktu paruh (t1/2) | Moda peluruhan | Produk | |
|---|---|---|---|---|---|
| 52Mn | syn | 5.591 d | ε | 52Cr | |
| β+ | 52Cr | ||||
| γ | – | ||||
| 53Mn | sisa | 3.74 ×106 y | ε | 53Cr | |
| 54Mn | syn | 312.3 d | ε | 54Cr | |
| γ | – | ||||
| 55Mn | 100% | 55Mn stabil dengan 30 neutron | |||
Sejarah Mangan
Pertama kali dikenali oleh Scheele, Bergman dan ahli lainnya sebagai unsur dandiisolasi oleh Gahn pada tahun 1774, dengan mereduksi mangan dioksida dengan karbon.
Efek Kesehatan Mangan

adalah unsur kimia dalam tabel periodik yang memiliki lambang Mn dan nomor atom 25.
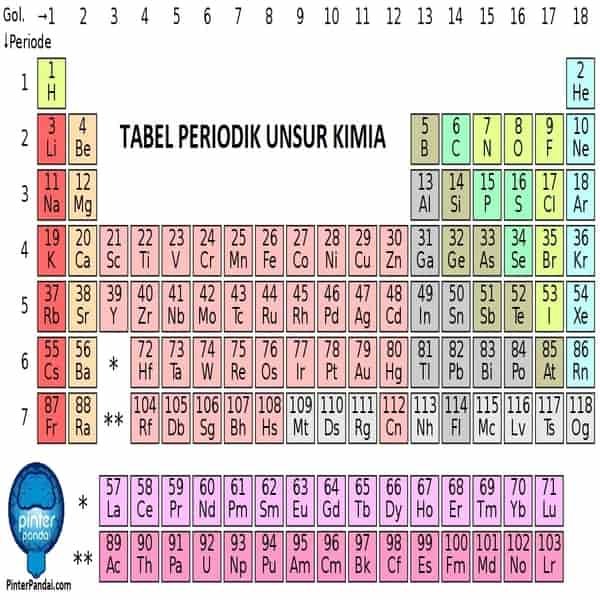
Tabel Periodik Kimia – Lengkap Dengan Daftar Unsur Kimia Berdasarkan Nama, Warna Dan Jenis
Tabel periodik adalah tampilan unsur-unsur kimia dalam bentuk tabel. Unsur-unsur tersebut disusun berdasarkan nomor atom (jumlah proton dalam inti atom), konfigurasi elektron dan keberulangan sifat kimia. Klik disini untuk membaca tabel periodik yang komplit.
Bacaan Lainnya
- Rumus Kimia Konsep Mol Dan Empiris Beserta Contoh Soal Dan Jawaban
- Manfaat Kalsium Untuk Tubuh Manusia
- Indonesia Juga Memiliki 3 Reaktor Nuklir
- Reaktor Nuklir Alami Zaman Purba
- Awalnya, reaktor nuklir pertama digunakan untuk produksi plutonium sebagai bahan senjata nuklir
- Top 10 Sungai Terpanjang Di Dunia
- Tes Kepribadian Warna & Warna Mana Yang Anda Miliki? Hijau, Oranye, Biru, Emas
- Kepalan Tangan Menandakan Karakter Anda & Kepalan nomer berapa yang Anda miliki?
- Tempat Wisata Yang Harus Dikunjungi Di Tokyo – Top 10 Obyek Wisata Yang Harus Anda Kunjungi
- Cara Membeli Tiket Pesawat Murah Secara Online Untuk Liburan Atau Bisnis
- Tibet Adalah Provinsi Cina – Sejarah Dan Budaya
- Puncak Gunung Tertinggi Di Dunia dimana?
- TOP 10 Gempa Bumi Terdahsyat Di Dunia
- Apakah Matahari Berputar Mengelilingi Pada Dirinya Sendiri?
- Test IPA: Planet Apa Yang Terdekat Dengan Matahari?
- 10 Cara Belajar Pintar, Efektif, Cepat Dan Mudah Di Ingat – Untuk Ulangan & Ujian Pasti Sukses!
- TOP 10 Virus Paling Mematikan Manusia
Unduh / Download Aplikasi HP Pinter Pandai
Respons “Ooo begitu ya…” akan lebih sering terdengar jika Anda mengunduh aplikasi kita!
Siapa bilang mau pintar harus bayar? Aplikasi Ilmu pengetahuan dan informasi yang membuat Anda menjadi lebih smart!
Sumber bacaan: Chemspider, National Center for Biotechnology Information, U.S. National Library of Medicine, Vanderkrogt
Pinter Pandai “Bersama-Sama Berbagi Ilmu”
Quiz | Matematika | IPA | Geografi & Sejarah | Info Unik | Lainnya